Article in the original language
Скільки грошей додатково отримає економіка, якщо ЄС погодить взаємне визнання GMP-сертифікатів, і чому це вигідно для обох сторін.
У 2022 році Україна експортувала в Євросоюз ліків на майже 39,5 млн дол. Ці показники були б значно вищими, якби не регуляторний бар’єр: відсутність визнання в ЄС українських сертифікатів GMP.
GMP-сертифікація (Good Manufacturing Practice – належна виробнича практика) – це підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики за міжнародними стандартами.
Мова йде про вимоги до персоналу, обладнання, приміщень, контролю якості, зберігання, пакування, маркування, відвантаження та дистрибуції ліків.
У 2022 році Україна експортувала в Євросоюз ліків на майже 39,5 млн дол. Ці показники були б значно вищими, якби не регуляторний бар’єр: відсутність визнання в ЄС українських сертифікатів GMP.
GMP-сертифікація (Good Manufacturing Practice – належна виробнича практика) – це підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики за міжнародними стандартами.
Мова йде про вимоги до персоналу, обладнання, приміщень, контролю якості, зберігання, пакування, маркування, відвантаження та дистрибуції ліків.
Скільки коштує конкуренція
Зараз для виходу на ринок Євросоюзу українські фармкомпанії проходять подвійну перевірку GMP: спочатку – в Україні, потім – на рівні держав-членів ЄС.
Крім основної сертифікації, існує процедура перевірки партії при ввезенні вантажів на територію ЄС – batch release. Це суттєво збільшує собівартість препаратів, що позначається на конкурентоздатності українських продуктів на ринках ЄС.
GMP-інспекція коштує 10-20 тис євро за виробництво. Такі інспекції відбуваються кожні два-три роки. На виробництві може бути сертифіковано кілька продуктів, але зазвичай для експорту до однієї країни ЄС інспектують три-чотири продукти. Тобто аудити проводяться не на весь портфель та виробничі лінії одного підприємства одночасно, що перешкоджає виходу нових українських продуктів на ринок ЄС.
У 2022 році Україна експортувала в Євросоюз ліків на майже 39,5 млн дол. Ці показники були б значно вищими, якби не регуляторний бар’єр: відсутність визнання в ЄС українських сертифікатів GMP.
GMP-сертифікація (Good Manufacturing Practice – належна виробнича практика) – це підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики за міжнародними стандартами.
Мова йде про вимоги до персоналу, обладнання, приміщень, контролю якості, зберігання, пакування, маркування, відвантаження та дистрибуції ліків.
Скільки коштує конкуренція
Зараз для виходу на ринок Євросоюзу українські фармкомпанії проходять подвійну перевірку GMP: спочатку – в Україні, потім – на рівні держав-членів ЄС.
Крім основної сертифікації, існує процедура перевірки партії при ввезенні вантажів на територію ЄС – batch release. Це суттєво збільшує собівартість препаратів, що позначається на конкурентоздатності українських продуктів на ринках ЄС.
GMP-інспекція коштує 10-20 тис євро за виробництво. Такі інспекції відбуваються кожні два-три роки. На виробництві може бути сертифіковано кілька продуктів, але зазвичай для експорту до однієї країни ЄС інспектують три-чотири продукти. Тобто аудити проводяться не на весь портфель та виробничі лінії одного підприємства одночасно, що перешкоджає виходу нових українських продуктів на ринок ЄС.
Вадим Шекман, “Добробут”: Міжнародна допомога Україні повинна відбуватися так, щоб не “вбити” місцеву економіку
Однак найвагоміший фактор у зростанні собівартості українських лікарських засобів при експорті в Євросоюз – процедура перевірки партії, що коштує в середньому 5 тис євро. Це додає в середньому 24% до собівартості продукту. Для недорогих препаратів збільшення собівартості може сягати 40-50%.
Додатково українські виробники сплачують послуги з трансферу аналітичних методик до лабораторії в ЄС, це ще близько 10 тис євро за кожен продукт. Якщо трансфер здійснюється в різні лабораторії (різним імпортерам), то кожного разу сплачується аналогічна сума, що теж впливає на собівартість товару.
Можемо заробляти майже вдвічі більш
Ми вирахували прогнозні об’єми постачання української лікарської продукції в ЄС за умови “фармбезвізу” – визнання Євросоюзом наших GMP-сертифікатів. За відправну точку розрахунків узяли 2025 рік. Аналіз демонструє, що за відсутності технічних бар’єрів для постачання лікарських засобів на європейські ринки у 2025 році експорт ліків може зрости на 30% від прогнозованого без “фармбезвізу”.
У 2026 році приріст сягне 35% відносно попереднього року, у 2027-2028 роках – на 25%. У 2029-2030 роках об’єми продажів лікарських засобів українського виробництва в країни ЄС будуть вищими на 18% відповідно до 2028-2029 років.
Таким чином, за прогнозами, у грошовому вираженні “фармбезвіз” виведе експорт українських ліків на рівень близько 100 млн дол у 2030 році. Якщо ж бар’єри залишаться, прогнозований експорт у ЄС у 2030 році становитиме 59 млн дол.
Що отримає економіка
Крім важливого для країни стабільного надходження валюти, у разі запровадження “фармбезвізу” прогнозується збільшення обсягів податків та числа робочих місць.
За оцінками експертів, з 2025 року податки від галузі можуть зрости на 30%. У держбюджет надійде на понад 800 тис дол більше. У 2030 році бюджет в умовах “фармбезвізу” може отримати 10,8 млн дол проти 6,4 млн дол без нього.
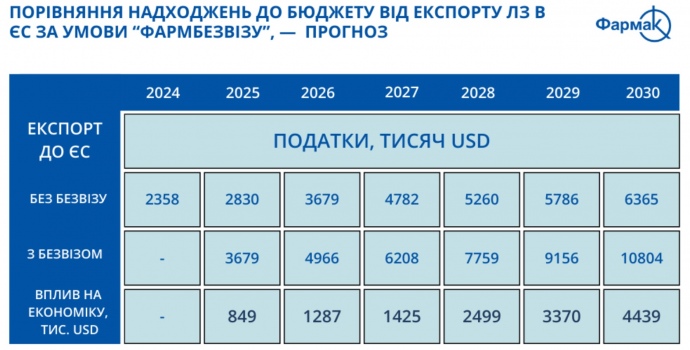
“Фармбезвіз” до 2030 року також забезпечить зростання робочих місць на українських підприємствах у 4,5 разу.
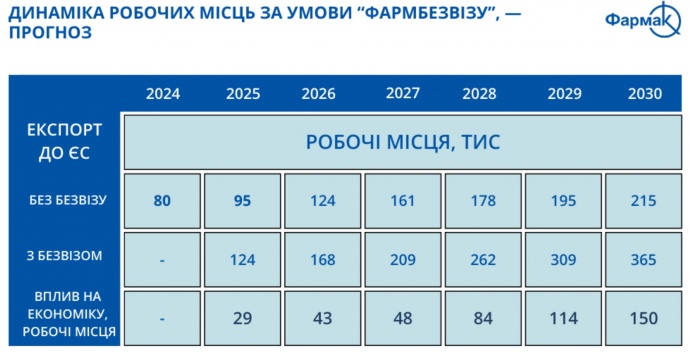
Чому зняття бар’єрів вигідне ЄС
Українські товари чи послуги не дуже хочуть бачити на ринках ЄС – недавні події з ринком зерна досі перед очима. Проте основні напрямки внутрішньої економічної політики ЄС включають управління стратегічними залежностями. Євросоюзу потрібна диверсифікація ланцюгів постачання та посилення індустріальної спроможності ЄС (ідеться про програму стратегічної автономії).
У галузі ліків Україна може зменшити залежність ЄС від виробництва й постачання активних фармацевтичних інгредієнтів (АФІ) та генеричних лікарських засобів з Індії та Китаю. Ми можемо виробляти АФІ, проміжні продукти та генеричні препарати з критичного переліку лікарських засобів Євросоюзу: антибіотики, тромболітики, інсулін, жарознижуючі, засоби для знеболення.
Провідні фармкомпанії України мають сучасні виробничі потужності, які дозволяють виготовляти лікарські засоби за контрактним виробництвом або трансфером технологій для внутрішнього ринку України, а також для експорту до регіону Центральної та Східної Європи, Центральної Азії та Кавказу.
Поки Міністерство охорони здоров’я, Верховна Рада та профільні бізнес-асоціації прискорюють виконання євроінтеграційних вимог для повної гармонізації із законодавством ЄС, з політичної точки зору м’яч зараз на боці Євросоюзу.
Колонка є видом матеріалу, який відображає винятково точку зору автора. Вона не претендує на об’єктивність та всебічність висвітлення теми, про яку йдеться. Точка зору редакції “Економічної правди” та “Української правди” може не збігатися з точкою зору автора. Редакція не відповідає за достовірність та тлумачення наведеної інформації і виконує винятково роль носія.